Starlix cukorbetegség kezelésére
Márkanév: Starlix
Általános név: nateglinid tabletta
Tartalom:
Leírás
Klinikai farmakológia
Klinikai vizsgálatok
Javallatok és felhasználás
Ellenjavallatok
óvintézkedések
Mellékhatások
túladagolás
Adagolás és adminisztráció
Hogyan szállították
Starlix, nateglinide, teljes betegtájékoztató (egyszerűen angolul)
Leírás
A Starlix® (nateglinid) egy orális antidiabetikum, amelyet a 2. típusú cukorbetegség kezelésére használnak [nem-inzulinfüggő diabetes mellitus (NIDDM) vagy felnőttkori diabéteszben is ismertek]. A Starlix, (-) - N - [(transz-4-izopropil-ciklohexán) -karbonil] -D-fenil-alanin szerkezetileg független az orális szulfonil-karbamid inzulin szekretagógokkal.
A szerkezeti képlet az ábrán látható
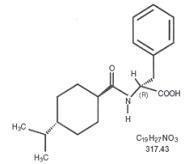
A Nateglinide fehér por, amelynek molekulatömege 317,43. Bőrben oldódik metanolban, etanolban és kloroformban, éterben oldódik, acetonitrilben és oktanolban csekély mértékben oldódik, és vízben gyakorlatilag nem oldódik. A Starlix bikonvex tabletta szájon át történő beadásra 60 mg vagy 120 mg nateglinidet tartalmaz.
Inaktív összetevők: kolloid szilícium-dioxid, kroszkarmellóz-nátrium, hidroxi-propil-metil-cellulóz, vas-oxidok (piros vagy sárga), laktóz-monohidrát, magnézium-sztearát, mikrokristályos cellulóz, polietilénglikol, povidon, talkum és titán dioxid.
felső
Klinikai farmakológia
A cselekvés mechanizmusa
A nateglinid egy aminosav-származék, amely csökkenti a vér glükózszintjét azáltal, hogy serkenti a hasnyálmirigy inzulinszekrécióját. Ez a hatás függ a hasnyálmirigy-szigetek működő béta-sejtjeitől. A nateglinid kölcsönhatásba lép az ATP-érzékeny kálium (K + ATP) csatornával a hasnyálmirigy béta-sejtjein. A béta-sejt ezt követő depolarizációja megnyitja a kalciumcsatornát, ami kalciumbeáramlást és inzulinszekréciót eredményez. Az inzulin felszabadulásának mértéke glükózfüggő, és alacsony glükózszint mellett csökken. A Nateglinide nagyon szövet-szelektív, alacsony affinitással rendelkezik a szívre és a csontváz izomra.
farmakokinetikája
Abszorpció
Közvetlenül étkezés előtt orális beadást követően a nateglinid gyorsan felszívódik, a plazma csúcskoncentrációja (Cmax) általában az adagolást követő 1 órán belül (Tmax) alakul ki. Ha 2-es típusú cukorbetegségben szenvedő betegeknek adják be a 60–240 mg dózistartományonként, naponta háromszor egyben A hét során a nateglinid lineáris farmakokinetikát mutatott mind az AUC (az idő / plazmakoncentráció görbe alatti terület), mind az AUC esetében Cmax. A Tmax szintén független volt a dózistól ebben a betegpopulációban. Az abszolút biohasznosulás becslések szerint körülbelül 73%. Étkezéskor vagy étkezés után adva a nateglinid felszívódása (AUC) nem változik. Ugyanakkor késleltethető a felszívódás sebessége, amelyet a Cmax csökkenése és a plazma csúcskoncentráció (Tmax) elérésének késleltetése jellemez. A plazmaprofilokat többszörös plazmakoncentráció-csúcsok jellemzik, ha a nateglinidet éhgyomri körülmények között adják be. Ez a hatás csökken, ha a nateglinidet étkezés előtt veszik be.
terjesztés
A nateglinid intravénás (IV) adagolását követő adatok alapján a nateglinid egyensúlyi állapotbeli megoszlási térfogata becslések szerint körülbelül 10 liter egészséges alanyokban. A nateglinid nagymértékben (98%) kötődik szérumfehérjékhez, elsősorban szérumalbuminhoz és kisebb mértékben Î ± 1 savas glikoproteinhez. A szérumfehérje-kötés mértéke független a gyógyszerkoncentrációtól a teszt 0,1-10 ug / ml tartományában.
Anyagcsere
A nateglinidet a kevert funkciós oxidáz rendszer metabolizálja az elimináció előtt. A metabolizmus fő útjai a hidroxiláció, amelyet a glükuronid konjugáció követ. A fő metabolitok kevésbé hatásos antidiabetikus szerek, mint a nateglinid. Az izoprén minor metabolit hasonló hatékonyságú, mint a nateglinid alapvegyületé.
In vitro adatok azt mutatják, hogy a nateglinidet túlnyomórészt citokróm P450 CYP2C9 (70%) és CYP3A4 (30%) izoenzimek metabolizálják.
Kiválasztás
A nateglinid és metabolitjai orális alkalmazás után gyorsan és teljesen eliminálódnak. Az adagolást követő 6 órán belül a beadott 14C-nateglinid kb. 75% -a visszanyert a vizeletben. A 14C-nateglinid nyolcvanhárom százaléka ürült a vizelettel, további 10% -a ürül a széklettel. A 14C-nateglinid körülbelül 16% -a ürül a vizelettel kiindulási vegyületként. Az egészséges önkéntesekkel és a 2. típusú cukorbetegségben szenvedő betegekkel végzett összes vizsgálatban a nateglinid plazmakoncentrációja gyorsan csökkent, átlagos eliminációs felezési ideje körülbelül 1,5 óra. E rövid eliminációs felezési idővel összhangban a nateglinid felhalmozódása nem észlelhető, ha napi háromszor, akár napi háromszor, 7 napon át többször adagolják a naglinlinidet.
Gyógyszerkölcsönhatások
In vitro gyógyszer-metabolizmus-vizsgálatok azt mutatják, hogy a Starlix-et főként a citokróm P450 CYP2C9 izoenzim (70%) és kisebb mértékben a CYP3A4 (30%) metabolizálja. A Starlix in vivo potenciálisan gátolja a CYP2C9 izoenzimet, amiről azt mutatja, hogy képes gátolni a tolbutamid in vitro metabolizmusát. A CYP3A4 metabolikus reakcióinak gátlását in vitro kísérletekben nem figyelték meg.
Glyburide: Egy randomizált, többdózisú kereszteződéses vizsgálatban 2-es típusú cukorbetegek voltak naponta háromszor 120 mg Starlix-et adunk be étkezés előtt 1 napig 10 gliceriddel kombinálva mg naponta. Egyik gyógyszer farmakokinetikájában sem volt klinikailag jelentős változás.
Metformin: Amikor a 120 mg Starlix-et napi háromszor étkezés előtt adják be, háromszor 500 mg metforminnal kombinálva Napi alkalommal 2-es típusú cukorbetegségben szenvedő betegek esetén sem a klinikailag releváns változások nem mutattak ki farmakokinetikában ügynök.
Digoxin: Amikor a Starlix 120 mg-ot étkezés előtt adták be egyetlen 1 mg-os adaggal együtt Az egészséges önkéntesek digoxin-tartalmát illetően, egyikükben sem történt klinikailag jelentős változás a farmakokinetikában ügynök.
Warfarin: Amikor az egészséges alanyoknak napi háromszor 120 mg Starlix-et adtak étkezés előtt, négy napig kombinációban egyszeri 30 mg warfarin adaggal a 2. napon, a farmakokinetikában sem volt változás ügynök. A protrombin idejét nem befolyásolta.
Diklofenak: A 120 mg Starlix reggeli és ebéd dózisának beadása egyetlen 75 mg-os adaggal kombinálva egészséges önkénteseknél a diklofenak adagja sem a farmakokinetikában sem változott szignifikánsan ügynök.
Különleges populációk
Geriatric: Az életkor nem befolyásolta a nateglinid farmakokinetikai tulajdonságait. Ezért az idős betegek esetében nincs szükség dózismódosításra.
Nem: Nem figyeltek meg klinikailag szignifikáns különbségeket a nateglinid farmakokinetikájában a férfiak és a nők között. Ezért nem szükséges a nemen alapuló adag módosítása.
Faj: A kaukázusi, fekete és más etnikai származású személyeket tartalmazó populáció farmakokinetikai elemzésének eredményei arra utalnak, hogy a faj kevés befolyást gyakorol a nateglinid farmakokinetikájára.
Vesekárosodás: Az egészséges egyezésű alanyokkal összehasonlítva, 2-es típusú cukorbetegségben szenvedő betegek és közepesen súlyos vagy súlyos veseelégtelenség (CrCl 15-50 ml / perc), nem dialízis alatt, hasonló nyilvánvalónak bizonyult clearance, AUC és Cmax. A dializált 2-es típusú cukorbetegségben és veseelégtelenségben szenvedő betegek összességében alacsonyabb expozíciót mutattak. A hemodializált betegekben azonban a plazmafehérje-kötődés csökkenése is tapasztalható, összehasonlítva az egészséges önkéntesekkel.
Májkárosodás: Az enyhe májelégtelenségben szenvedő, nem diabéteszes betegekben a nateglinid csúcsértéke és teljes expozíciója 30% -kal nőtt az egyező egészséges alanyokhoz képest. A Starlix®-t (nateglinid) óvatosan kell alkalmazni krónikus májbetegségben szenvedő betegek esetén. (Lásd ÓVINTÉZKEDÉSEK, Májkárosodás.)
Gyógyszerhatástani
A Starlix gyorsan felszívódik és stimulálja a hasnyálmirigy inzulin kiválasztását az orális beadást követő 20 percen belül. Ha a Starlix-et naponta háromszor adagolják étkezés előtt, a plazma inzulin gyorsan emelkedik, a csúcsszint kb. 1 órával az adagolás után, és az alapértékhez esik az adagolás után 4 órával.
Kettős-vak, kontrollált klinikai vizsgálatban, amelyben a Starlix-et három mindegyik előtt adták be étkezés után a plazma glükózszintet 12 órás napi periódusban határozták meg 7 hetes után kezelés. A Starlix-t 10 perccel étkezés előtt adták be. Az étkezések a szokásos diabéteszes súlymegtartó menük alapján készültek, az összes kalóriatartalom alapján az egyes alanyok magassága alapján. A Starlix statisztikailag szignifikáns csökkenést okozott az éhomi és étkezés utáni glikémiában a placebohoz képest.
felső
Klinikai vizsgálatok
Összesen 3566 beteget randomizáltak kilenc kettős-vak, placebo- vagy aktív kontrollos, 8–24 hetes vizsgálatban a Starlix® (nateglinid) biztonságosságának és hatékonyságának értékelésére. 3513 beteg hatékonysági értékei meghaladták a kiindulási értéket. Ezekben a vizsgálatokban a Starlix-et legfeljebb 30 perccel adták be napi három fő étkezés előtt.
A Starlix® monoterápia a placebohoz képest
Egy randomizált, kettős-vak, placebo-kontrollos, 24 hetes vizsgálatban HbA1C-vel szenvedő, 2. típusú cukorbetegségben szenvedő betegek â ‰ 8 6,8% -a önmagában étrendben randomizálták a Starlix-ot (napi háromszor 60 mg vagy 120 mg étkezés előtt) vagy placebót. A kiindulási HbA1C 7,9% és 8,1% között volt, és a betegek 77,8% -a volt korábban nem kezelt orális antidiabetikus kezeléssel. A korábban antidiabetikus gyógyszerekkel kezelt betegeknek a véletlenszerű besorolás előtt legalább 2 hónappal abba kellett hagyniuk a gyógyszer szedését. A Starlix étkezés előtti hozzáadása statisztikailag szignifikáns csökkenést eredményezett az átlagos HbA1C és az éhomi plazma glükóz (FPG) összehasonlításában a placebóval összehasonlítva (lásd az 1. táblázatot). A HbA1C és az FPG csökkenése hasonló volt azoknál a betegeknél, akiknél még nem voltak antidiabetikumok.
Ebben a tanulmányban súlyos hypoglykaemia egy epizódjáról (plazma glükóz <36 mg / dL) számoltak be egy betegnél, aki napi háromszor 120 mg Starlix-kel kezelt étkezés előtt. Egyik betegnél sem fordult elő hypoglykaemia, amely harmadik személyek segítségét igényelte. A Starlix-szel kezelt betegek statisztikailag szignifikáns átlagos növekedést mutattak a placebóhoz képest (lásd 1. táblázat).
Egy másik randomizált, kettős-vak, 24-hetes, aktív és placebo-kontrollos vizsgálatban a 2. típusú cukorbetegségben szenvedő betegeket randomizálták Starlix-kezeléssel (háromszor 120 mg). naponta étkezés előtt), 500 mg metformin (naponta háromszor), a 120 mg Starlix (étkezés előtt háromszor háromszor) és az 500 mg metformin (naponta háromszor) kombinációjával, vagy placebo. A kiindulási HbA1C 8,3% és 8,4% között volt. A betegek 57% -át már nem kezelték orális antidiabetikus kezeléssel. A Starlix monoterápia az átlagos HbA1C és az átlagos FPG szignifikáns csökkenését eredményezte a placebohoz képest, hasonlóak a fentiekben ismertetett vizsgálat eredményeihez (lásd a 2. táblázatot).
1. táblázat: A Starlix® monoterápia 24 hetes, fix dózisú vizsgálat végpont eredményei
|
Placebo |
Starlix® 60 mg háromszor napi étkezések előtt |
Starlix® 120 mg háromszor napi étkezések előtt |
|
| HbA1C (%) | N = 168 | N = 167 | N = 168 |
| Alapvonal (átlag) | 8.0 | 7.9 | 8.1 |
| Változás a kiindulási értékhez képest (átlag) | +0.2 | -0.3 | -0.5 |
| Különbség a placebótól (átlag) | -0.5 egy | -0.7 egy | |
| FPG (mg / dL) | N = 172 | N = 171 | N = 169 |
| Alapvonal (átlag) | 167.9 | 161.0 | 166.5 |
| Változás a kiindulási értékhez képest (átlag) | +9.1 | +0.4 | -4.5 |
| Különbség a placebótól (átlag) | -8.7 egy | -13.6 egy | |
| Súly (kg) | N = 170 | N = 169 | N = 166 |
| Alapvonal (átlag) | 85.8 | 83.7 | 86.3 |
| Változás a kiindulási értékhez képest (átlag) | -0.7 | +0.3 | +0.9 |
| Különbség a placebótól (átlag) | +1.0 egy | +1.6 egy |
p-érték â ‰ ¤ 0,004
A Starlix® monoterápia összehasonlítva más orális antidiabetikumokkal
gliburidot
Egy 24 hetes, kettős-vak, aktív kontrollos vizsgálatban olyan 2-es típusú cukorbetegségben szenvedő betegeket, akik 3 hónapon át szulfonilurea-kezelésben részesültek, és akik a kiindulási HbA1C értéke - 6,5% volt véletlenszerűen kiválasztva Starlix (napi háromszor 60 mg vagy 120 mg étkezés előtt) vagy 10 mg glicurid egyszeri kapására. napi. A Starlix-ra randomizált betegek szignifikáns emelkedése volt az átlagos HbA1C és az átlagos FPG-ben a végpontban, összehasonlítva a gluturiddal randomizált betegekkel.
metformin
Egy másik randomizált, kettős-vak, 24-hetes, aktív és placebo-kontrollos vizsgálatban a 2. típusú cukorbetegségben szenvedő betegeket randomizálták Starlix-kezeléssel (háromszor 120 mg). naponta étkezés előtt), 500 mg metformin (naponta háromszor), a 120 mg Starlix (étkezés előtt háromszor háromszor) és az 500 mg metformin (naponta háromszor) kombinációjával, vagy placebo. A kiindulási HbA1C 8,3% és 8,4% között volt. A betegek 57% -át már nem kezelték orális antidiabetikus kezeléssel. Az átlagos HbA1C és az átlagos FPG csökkenése a végpontnál metformin monoterápiával szignifikánsan nagyobb volt, mint ezekben a változókban a Starlix monoterápiával történő csökkenése (lásd 2. táblázat). A placebóhoz viszonyítva a Starlix monoterápiát az átlagtömeg szignifikáns növekedésével társították, míg a metformin monoterápiát az átlagtömeg szignifikáns csökkenésével társították. Az antidiabetikus terápiával nem kezelt betegek körében az átlagos HbA1C és az átlagos FPG csökkenése a Starlix monoterápiában hasonló volt a metformin monoterápiánál (lásd 2. táblázat). A Starlix-ben korábban más antidiabetikus szerekkel, elsősorban glicuriddal, HbA1C-vel kezelt betegek körében A monoterápiás csoport kissé emelkedett a kiindulási értékhez képest, míg a HbA1C csökkent a metformin monoterápiás csoportban (lásd a 4. táblázatot) 2).
Starlix® kombinációs terápia
metformin
Egy másik randomizált, kettős-vak, 24-hetes, aktív és placebo-kontrollos vizsgálatban a 2. típusú cukorbetegségben szenvedő betegeket randomizálták Starlix-kezeléssel (háromszor 120 mg). naponta étkezés előtt), 500 mg metformin (naponta háromszor), a 120 mg Starlix (étkezés előtt háromszor háromszor) és az 500 mg metformin (naponta háromszor) kombinációjával, vagy placebo. A kiindulási HbA1C 8,3% és 8,4% között volt. A betegek 57% -át már nem kezelték orális antidiabetikus kezeléssel. A korábban antidiabetikumokkal kezelt betegeknek a randomizáció előtt legalább 2 hónappal abba kellett hagyniuk a gyógyszeres kezelést. A Starlix és a metformin kombinációja statisztikailag szignifikánsan nagyobb mértékű HbA1C és FPG csökkenést eredményezett a Starlix vagy a metformin monoterápiához képest (lásd a 2. táblázatot). A Starlix önmagában vagy metforminnal kombinálva szignifikánsan csökkentette az étkezés előtti gyakorlati glükózszint emelkedést az étkezés utáni 2 órára, összehasonlítva a placebóval és a metforminval önmagában.
Ebben a tanulmányban a súlyos hypoglykaemia egy epizódjáról (plazma glükóz - 36 mg / dl) számoltak be egy a Starlix és a metformin kombinációjáról, valamint négy súlyos hypoglykaemia epizódról számoltak be egyetlen metforminos betegnél kezelési kar. Egyetlen beteg sem tapasztalt olyan hypoglykaemia epizódot, amely harmadik személyek segítségét igényelte. A placebóval összehasonlítva a Starlix monoterápiát statisztikailag szignifikáns súlynövekedéssel társították, míg a Starlix és a metformin kombinált kezeléssel nem figyeltünk meg szignifikáns súlyváltozást (lásd 2. táblázat).
Egy másik 24 hetes, kettős vak, placebo-kontrollos vizsgálatban először a metformin-kezelést követően (2 havonta 1500 mg naponta, 1 hónapig) a HbA1C-ben szenvedő, 2-es típusú cukorbetegségben szenvedő betegek (6,5% -a) kezdetét vették be A metformin monoterápia négyhetes beadási periódusa (napi 2000 mg), majd véletlenszerűen kiválasztva Starlix-et (napi háromszor 60 mg vagy 120 mg étkezés előtt) vagy placebót kap a metformin mellett. A Starlix és a metformin kombinációs terápia statisztikailag szignifikánsan nagyobb mértékű csökkenését okozta HbA1C összehasonlítva a metformin monoterápiával (-0,4% és -0,6% a 60 mg Starlix és a 120 mg Starlix plusz metformin mellett, illetőleg).
2. táblázat: A Starlix® monoterápia és a metformin kombinációjának 24 hetes vizsgálatának végeredményei
|
Placebo |
Starlix® 120 mg háromszor minden nap előtte ételek |
metformin 500 mg háromszor napi |
Starlix® 120 mg előtt étkezés plusz metformin * |
|
| HbA1C (%) | ||||
| Összes | N = 160 | N = 171 | N = 172 | N = 162 |
| Alapvonal (átlag) | 8.3 | 8.3 | 8.4 | 8.4 |
| Változás a kiindulási értékhez képest (átlag) | +0.4 | -0.4 időszámításunk előtt | -0.8 c | -1.5 |
| Különbség a placebótól | -0.8 egy | -1.2 egy | -1.9 egy | |
| Nan-ve | N = 98 | N = 99 | N = 98 | N = 81 |
| Alapvonal (átlag) | 8.2 | 8.1 | 8.3 | 8.2 |
| Változás a kiindulási értékhez képest (átlag) | +0.3 | -0.7 c | -0.8 c | -1.6 |
| Különbség a placebótól | -1.0 egy | -1.1 egy | -1.9 egy | |
| Nem Nan-ve | N = 62 | N = 72 | N = 74 | N = 81 |
| Alapvonal (átlag) | 8.3 | 8.5 | 8.7 | 8.7 |
| Változás a kiindulási értékhez képest (átlag) | +0.6 | +0.004 időszámításunk előtt | -0.8 c | -1.4 |
| Különbség a placebótól | -0.6 egy | -1.4 egy | -2.0 egy | |
| FPG (mg / dL) | ||||
| Összes | N = 166 | N = 173 | N = 174 | N = 167 |
| Alapvonal (átlag) | 194.0 | 196.5 | 196.0 | 197.7 |
| Változás a kiindulási értékhez képest (átlag) | +8.0 | -13.1 időszámításunk előtt | -30.0 c | -44.9 |
| Különbség a placebótól | -21.1 egy | -38.0 egy | -52.9 egy | |
| Súly (kg) | ||||
| Összes | N = 160 | N = 169 | N = 169 | N = 160 |
| Alapvonal (átlag) | 85.0 | 85.0 | 86.0 | 87.4 |
| Változás a kiindulási értékhez képest (átlag) | -0.4 | +0.9 időszámításunk előtt | -0.1 | +0.2 |
| Különbség a placebótól | +1.3 egy | +0.3 | +0.6 |
p-érték: 0,05 vs. placebo
b p-érték: 0,03 vs. metformin
c p-érték - 0,05 vs. kombináció
* A metforminot naponta háromszor adták be
roziglitazon
24 hetes, dupla vak, multicentrikus, placebo-kontrollos vizsgálatot végeztünk 2. típusú betegekkel cukorbetegség, a 8 mg roziglitazon monoterápiára adott terápiás válasz után nem szabályozható megfelelően napi. A Starlix adagolása (napi háromszori 120 mg étkezés közben) hozzáadása statisztikailag szignifikánsan nagyobb HbA1C csökkenéshez kapcsolódott, mint a rosiglitazon monoterápia. A különbség -0,77% volt a 24. héten. A Starlix plusz roziglitazonnal kezelt betegek átlagos súlyváltozása az alapszinthez képest körülbelül +3 kg volt, míg a placeboval és roziglitazonnal kezelt betegek esetében körülbelül +1 kg.
gliburidot
Egy 2 hetes típusú cukorbetegségben szenvedő betegek 12 hetes vizsgálatában, melynek napi egyszeri 10 mg-os glicurid kezelése nem volt megfelelő a Starlix adagolása (napi háromszor 60 mg vagy 120 mg étkezés előtt) nem eredményezett újabb mennyiséget haszon.
felső
Javallatok és felhasználás
A Starlix® (nateglinid) étrend és testmozgás kiegészítéseként javasolt, hogy javítsa a 2-es típusú diabetes mellitusban szenvedő felnőttek glikémiás kontrollját.
felső
Ellenjavallatok
A Starlix® (nateglinid) ellenjavallt az alábbi betegek esetén:
1. Ismert túlérzékenység a gyógyszerrel vagy annak inaktív összetevőivel szemben.
2. 1. típusú cukorbetegség.
3. Cukorbetegség során jelentkező acetonsav felszaporodás a szervezetben. Ezt az állapotot inzulinnal kell kezelni.
felső
óvintézkedések
Makrovaszkuláris eredmények: Nincs klinikai vizsgálat, amely meggyőző bizonyítékot szolgáltatna a makrovaszkuláris kockázat csökkentésére a Starlix vagy bármely más antidiabetikus gyógyszer esetén.
Hipoglikémia: Az összes szisztémásán felszívódott orális vércukorszint-csökkentő gyógyszer képes hipoglikémiát okozni. A hipoglikémia gyakorisága függ a cukorbetegség súlyosságától, a glikémiás kontroll szintjétől és a beteg egyéb jellemzőitől. A geriatrikus betegek, az alultáplált betegek, valamint mellékvese- vagy hipofízis elégtelenség vagy súlyos vesekárosodás esetén érzékenyebbek ezeknek a kezeléseknek a glükózcsökkentő hatása. A hipoglikémia kockázatát növelheti az erőteljes testmozgás, az alkoholfogyasztás, elégtelen kalóriabevitel akut vagy krónikus alapon, vagy más orális antidiabetikumokkal történő kombináció szerek. A hipoglikémiát nehéz lehet felismerni autonóm neuropathiában szenvedő és / vagy béta-blokkolókat használó betegek körében. A Starlix®-t (nateglinid) étkezés előtt kell beadni a hipoglikémia kockázatának csökkentése érdekében. Az étkezést kihagyó betegeknek ki kell hagyniuk a Starlix tervezett adagját is a hipoglikémia kockázatának csökkentése érdekében.
Májkárosodás: A Starlix-t óvatosan kell alkalmazni közepesen súlyos vagy súlyos májbetegségben szenvedő betegekben, mivel ezeket a betegeket nem vizsgálták.
A glikémiás kontroll elvesztése
A glikémiás kontroll átmeneti elvesztése láz, fertőzés, trauma vagy műtét következtében fordulhat elő. Ilyenkor az inzulinterápiára lehet szükség a Starlix terápia helyett. Másodlagos meghibásodás vagy a Starlix hatékonysága egy bizonyos ideig csökkenhet.
Információ a betegek számára
A betegeket tájékoztatni kell a Starlix lehetséges kockázatairól és előnyeiről, valamint az alternatív terápiás módokról. Meg kell magyarázni a hipoglikémia kockázatait és kezelését. A betegeket fel kell utasítani arra, hogy 1-30 perccel az étkezés bevétele előtt vegyék be a Starlix-et, de az étkezés kihagyásakor hagyják ki az ütemezett adagot, hogy csökkenjen a hypoglykaemia kockázata. A gyógyszerkölcsönhatásokat meg kell beszélni a betegekkel. A betegeket tájékoztatni kell a Starlix-szel való lehetséges gyógyszer-interakciókról.
Laboratóriumi tesztek
A terápiára adott válaszokat időszakonként kell értékelni a glükózértékek és a HbA1C szint alapján.
Gyógyszerkölcsönhatások
A nateglinid nagymértékben kötődik plazmafehérjékhez (98%), főként albuminhoz. In vitro eltolódási vizsgálatok erősen fehérjéhez kötött gyógyszerekkel, például furoszemiddel, propranolollal, kaptoprillal, nikardipinnel, pravasztatinval, a gliburid, warfarin, fenitoin, acetil-szalicilsav, tolbutamid és metformin nem befolyásolta a nateglinid fehérje mennyiségét kötés. Hasonlóképpen, a nateglinid nem befolyásolta a propranolol, glicurid, nikardipin, warfarin, fenitoin, acetil-szalicilsav és tolbutamid szérumfehérje-kötődését in vitro. Az egyes esetek körültekintő értékelése azonban a klinikai körülmények között indokolt.
Egyes gyógyszerek, beleértve a nem szteroid gyulladásgátlókat (NSAID-ok), szalicilátok, monoamin-oxidáz inhibitorok és nem szelektív béta-adrenerg blokkoló szerek fokozhatják a Starlix és más orális antidiabetikumok hipoglikémiás hatását gyógyszerek.
Bizonyos gyógyszerek, beleértve a tiazidokat, kortikoszteroidokat, pajzsmirigytermékeket és szimpatomimetikumokat, csökkenthetik a Starlix és más orális antidiabetikumok hipoglikémiás hatását.
Amikor ezeket a gyógyszereket a Starlix-et kapó betegeknek adják be vagy vonják ki, a beteget szorosan meg kell figyelni a glikémiás kontroll változásainak alakulása szempontjából.
Gyógyszer / élelmiszer kölcsönhatások
A nateglinid farmakokinetikáját az étkezés összetétele nem befolyásolta (magas protein, zsír vagy szénhidrát). A csúcs plazmaszintje azonban jelentősen csökkent, amikor a Starlix-et 10 perccel a folyékony étkezés előtt adták be. A Starlix nem befolyásolta az egészséges alanyok gyomorürülését az acetaminofén tesztelés alapján.
Karcinogenezis / Mutagenezis / A termékenység romlása
Karcinogenitás: Két éves karcinogenitási vizsgálatot végeztek Sprague-Dawley patkányokban nateglinid orális dózisával, napi 900 mg / kg-ig, ami AUC-expozíciót eredményezett hím és nőstény patkányokban a humán terápiás expozíció körülbelül 30-szorosával és 40-szeresével, ajánlott 120 mg Starlix-adaggal, napi háromszor, mielőtt ételek. Kétéves karcinogenitási vizsgálatot végeztek B6C3F1 egerekben nateglinid orális dózisaival, napi 400 mg / kg-ig, ami AUC-expozíciót eredményezett hím férfiakon és nőstény egerek kb. 10 és 30-szorosa a humán terápiás expozíciónak, az ajánlott 120 mg Starlix-adaggal, napi háromszor étkezés előtt. Patkányokban vagy egerekben nem találtak tumorogén válaszreakciót.
Mutagenezis: A Nateglinid nem volt genotoxikus az in vitro Ames tesztben, az egér limfóma vizsgálatban, a kromoszóma aberrációs vizsgálatban a kínai hörcsög tüdősejtekben vagy az in vivo egér mikronukleusz tesztben.
A termékenység romlása: A termékenységet nem befolyásolta a nateglinid patkányokon történő adagolása, legfeljebb 600 mg / kg dózisban. (körülbelül a humán terápiás expozíció körülbelül tizenszerese a napi háromszor ajánlott 120 mg Starlix-adaggal ételek).
Terhesség
C terhességi kategória
A nateglinid nem volt teratogén patkányokban, 1000 mg / kg-nál magasabb dózisok mellett (kb. 60-szorosa a humán terápiás expozíciónak, ha a Starlix ajánlott adagja 120 mg, napi háromszor étkezés előtt). A nyulakban az embrionális fejlődést hátrányosan befolyásolták, és az epehólyag agenesis vagy a kicsi epehólyag incidenciája megnőtt 500 mg / kg dózis (körülbelül a humán terápiás expozíció körülbelül 40-szerese a javasolt 120 mg Starlix-adaggal, napi háromszor, mielőtt ételek). Terhes nőkön nincs megfelelő és jól ellenőrzött vizsgálat. A Starlix nem alkalmazható terhesség alatt.
Munka és szállítás
A Starlix emberi fogamzásra és szülésre gyakorolt hatása nem ismert.
Szoptató anyák
Szoptató patkányokkal végzett vizsgálatok azt mutatták, hogy a nateglinid kiválasztódik a tejbe; a tej és a plazma AUC0-48h aránya körülbelül 1: 4 volt. A peri- és postnatális időszakban a testtömeg alacsonyabb volt az olyan patkányok utódjain, akiknek nateglinidet adtak 1000 mg / kg-os adagban. (kb. 60-szorosa a humán terápiás expozíciónak, az ajánlott 120 mg Starlix-adaggal, napi háromszor azelőtt ételek). Nem ismert, hogy a Starlix kiválasztódik-e az anyatejbe. Mivel sok gyógyszer kiválasztódik az anyatejbe, a Starlix-et nem szabad szoptató nőnek adni.
Gyermekgyógyászati alkalmazás
A Starlix biztonságosságát és hatékonyságát gyermekkori betegekben nem igazolták.
Geriatric használat
A Starlix biztonságosságában vagy hatékonyságában nem mutattak különbséget a 65 éves és annál idősebb betegek, valamint a 65 év alatti betegek között. Ugyanakkor nem zárható ki néhány idõsebb személy nagyobb szenzitivitása a Starlix kezelés ellen.
felső
Mellékhatások
A klinikai vizsgálatok során körülbelül 2600 2. típusú cukorbetegségben szenvedő beteget kezeltek Starlix®-vel (nateglinid). Ezek közül körülbelül 1335 beteget kezeltek legalább 6 hónapig, körülbelül 190 beteget egy vagy annál hosszabb ideig.
A hipoglikémia viszonylag ritka volt a klinikai vizsgálatok összes kezelési ágában. A Starlix-betegeknek csak 0,3% -a hagyta abba a hipoglikémia miatt. A gyomor-bélrendszeri tünetek, különösen a hasmenés és émelygés nem voltak gyakoribbak a Starlix és a metformin kombinációját alkalmazó betegekben, mint azokban a betegekben, akiket csak metformin kaptak. Hasonlóképpen, a perifériás ödéma nem gyakrabban fordult elő a Starlix és a rosiglitazon kombinációját alkalmazó betegekben, mint azokban a betegekben, akik csak a rosiglitazonot kapják. Az alábbi táblázat felsorolja azokat az eseményeket, amelyek ellenőrzött klinikai vizsgálatokban gyakrabban fordultak elő Starlix-betegekben, mint a placebo-betegekben.
Gyakori nemkívánatos események (Star%% 2% Starlix® betegekben) a Starlix® monoterápiás vizsgálatokban (a betegek% -a)
| Placebo | Starlix® | |
| N = 458 | N = 1441 | |
| Előnyben részesített kifejezés | ||
| Felső légúti fertőzés | 8.1 | 10.5 |
| Hátfájás | 3.7 | 4.0 |
| Influenza tünetei | 2.6 | 3.6 |
| Szédülés | 2.2 | 3.6 |
| arthropathia | 2.2 | 3.3 |
| Hasmenés | 3.1 | 3.2 |
| Véletlen trauma | 1.7 | 2.9 |
| Hörghurut | 2.6 | 2.7 |
| Köhögés | 2.2 | 2.4 |
| A hipoglikémia | 0.4 | 2.4 |
A forgalomba hozatal utáni tapasztalatok során ritka esetekben számoltak be túlérzékenységi reakciókról, mint például kiütés, viszketés és csalánkiütés. Hasonlóképpen, sárgaság, kolesztatikus hepatitis és emelkedett májenzimek eseteiről számoltak be.
Laboratóriumi rendellenességek
Húgysav: A csak Starlix-szel, a Starlix-rel metforminnal, önmagában metforminnal és önmagában a glicuriddal kezelt betegek átlagos húgysavszintje emelkedett. A placebóhoz viszonyított különbségek 0,29 mg / dL, 0,45 mg / dL, 0,28 mg / dL és 0,19 mg / dL. Ezen eredmények klinikai jelentősége nem ismert.
felső
túladagolás
A 2. típusú cukorbetegségben szenvedő betegek klinikai vizsgálatában a Starlix®-t (nateglinid) adták be az adagok napi 720 mg-ig történő növelése 7 napig, és nem voltak klinikailag szignifikáns mellékhatások számoltak be. A klinikai vizsgálatok során a Starlix túladagolása nem fordult elő. A túladagolás azonban túlzott glükózszint-csökkentő hatást eredményezhet a hipoglikémiás tünetek kialakulásával. A hipoglikémiás tüneteket eszméletvesztés vagy neurológiai leletek nélkül, orális glükózzal és az adagolás és / vagy étkezési szokások kiigazításával kell kezelni. Kómával, rohamokkal vagy más neurológiai tünetekkel járó súlyos hipoglikémiás reakciókat intravénás glükózzal kell kezelni. Mivel a nateglinid nagymértékben kötődik a fehérjékhez, a dialízis nem hatékony eszköz a vérből történő eltávolításához.
felső
Adagolás és adminisztráció
A Starlix®-t (nateglinid) étkezés előtt 1-30 perccel kell bevenni.
Monoterápia és kombináció metforminnal vagy tiazolidindionnal
A Starlix ajánlott kezdő és fenntartó adagja önmagában vagy metforminnal vagy tiazolidindionnal kombinálva napi háromszor, étkezés előtt.
A Starlix 60 mg-os adagja önmagában vagy metforminnal vagy tiazolidindionnal kombinálva alkalmazható olyan betegekben, akik a kezelés megkezdésekor a HbA1C cél közelében vannak.
Adagolás geriatrikus betegekben
Különleges dózismódosításra nincs szükség. Ugyanakkor nem zárható ki egyes egyének nagyobb érzékenysége a Starlix-kezeléssel szemben.
Adagolás vese- és májkárosodásban
Enyhe-súlyos veseelégtelenségben vagy enyhe májelégtelenségben nem szükséges az adag módosítása. Közepesen súlyos vagy súlyos májelégtelenségben szenvedő betegek adagolását nem vizsgálták. Ezért a Starlix-t óvatosan kell alkalmazni közepesen súlyos vagy súlyos májbetegségben szenvedő betegek esetén (lásd ÓVINTÉZKEDÉSEK, Májkárosodás).
felső
Hogyan szállították
Starlix® (nateglinid) tabletta
60 mg
Rózsaszín, kerek, ferde széllel rendelkező tabletta, egyik oldalán "Starlix", a másik oldalán "60".
Palack 100... NDC 0078-0351-05
120 mg
Sárga, ovális tabletta, egyik oldalán "Starlix", másik oldalán "120" betűvel.
Palack 100... NDC 0078-0352-05
Tárolás
Tárolja 25 ° C-on (77 ° F); kirándulások megengedettek 15 ºC-30 ºC-ra (59 ºF-86 ºF).
Kiadjuk szűk tartályban, USP.
T2008-01
REV: 2008. JÚLIUS
Készítette:
Novartis Pharma Stein AG
Stein, Svájc
Forgalmazza:
Novartis Pharmaceuticals Corporation
Kelet-Hanover, New Jersey 07936
© Novartis
Utoljára frissítve: 2008.07.07
Starlix, nateglinide, teljes betegtájékoztató (egyszerűen angolul)
Részletes információ a cukorbetegség jeleiről, tüneteiről, okairól, kezeléséről
Az ebben a monográfiában szereplő információknak nem célja az összes lehetséges felhasználás, utasítások, óvintézkedések, gyógyszerkölcsönhatások vagy káros hatások lefedése. Ez az információ általános, és nem célja speciális orvosi tanácsadás. Ha kérdése van a használt gyógyszerekkel kapcsolatban, vagy további információt szeretne, keresse fel orvosát, gyógyszerészét vagy ápolóját.
vissza a: Keresse meg a cukorbetegség kezelésére szolgáló összes gyógyszert



